研究内容
1. 材料体系设计与粘附机制
研究团队开发了一种基于接枝互穿网络的聚合物体系:由N-羟基琥珀酰亚胺酯(NHS)功能化的聚丙烯酸(PAA-NHS),与亲水聚氨酯(PU)互穿并接枝,形成PU-PAA-NHS聚合物网络。
粘附机制:
① 快速除水:PAA链的高浓度带电羧酸基团可快速吸收界面水,配合网格孔隙的毛细管作用,数秒内清除粘合剂-组织界面的水分,实现与湿组织的快速贴合;
② 化学键合:NHS酯基团可与组织表面的伯胺反应形成共价酰胺键,实现稳定的界面结合;
③ 能量耗散:PU中的硬段通过动态氢键相互作用,在形变过程中提供高效的能量耗散机制,大幅提升材料的粘附韧性与拉伸性能。
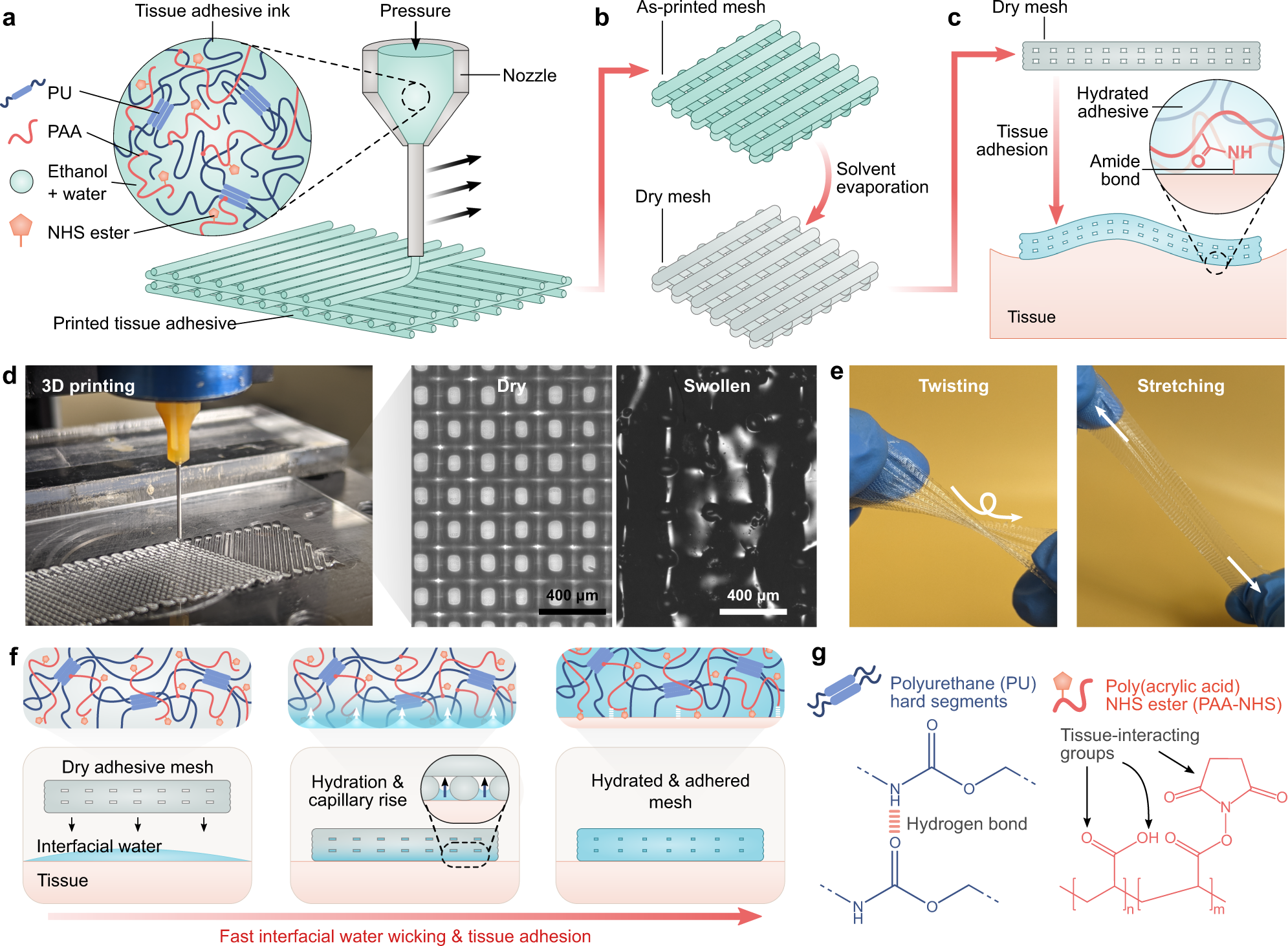
d:3D打印过程照片,以及干燥和溶胀状态下3D打印网格贴片的显微照片;
e:打印后的贴片被扭曲和拉伸的照片,展现优异的柔性与拉伸性;
f:粘附机制示意图,通过材料水合和网格孔隙的毛细作用快速清除界面水,实现与组织的快速结合,通过分子间作用力和共价键稳定粘附效果;
g:3D可打印组织粘合剂共聚物的关键化学基团:聚氨酯(PU)中的氢键形成基团,以及聚丙烯酸(PAA)上与NHS酯偶联的组织相互作用基团。
2. 材料合成与可打印性优化
采用光引发聚合法实现PU-PAA接枝互穿网络的一步法合成:在含有PU、丙烯酸(AA)、α-酮戊二酸和二苯甲酮的溶液中,通过紫外光激活聚合反应。其中α-酮戊二酸作为AA聚合的引发剂,二苯甲酮则在PU上产生自由基位点,实现PAA向PU的共价接枝。
通过透析纯化产物后,利用EDC偶联剂对PAA链进行NHS酯功能化,实现约10%的羧酸基团NHS功能化,最终制备打印墨水。
打印性能优化:
① 浓度优化:总聚合物浓度低于15 w/w%的墨水易铺展,形状保真度差;高于25 w/w%的墨水易堵塞喷嘴,难以挤出;最优配方为15 w/w% PU-PAA + 5 w/w% PU,具备优异的打印适配性;
② 流变性能:墨水具备显著的剪切变稀行为,可通过200μm喷嘴顺利挤出,挤出后可保持形状,实现稳定的层叠打印;
③ 精度调控:可通过调整挤出压力和打印头速度,精准控制丝径和孔隙尺寸,实现可编程的结构设计。

b-c:不同前驱体组成制备材料的FTIR光谱,验证了PAA的成功接枝;
d:不同NHS功能化程度的组织粘合剂样品的1H NMR光谱;
e:不同聚合物浓度的组织粘合剂墨水的表观粘度随剪切速率的变化,展现剪切变稀特性;
f:不同聚合物浓度墨水的剪切储能模量随剪切应力的变化;
g:丝宽随打印速度的变化规律,验证了打印精度的可控性。
3. 粘附性能与力学可调性表征
研究团队对打印后的粘合剂贴片进行了系统的性能测试,核心性能指标远超商用产品:
| 性能指标 | 本研究3D打印粘合剂 | 商用产品对标 |
|---|---|---|
| 湿组织界面韧性 | >300 J·m⁻² | 显著优于Coseal、TachoSil、Tegaderm |
| 粘附剪切强度 | >75 kPa | 远超商用产品水平 |
| 爆破压力 | >26 kPa | 高于高血压收缩压(17-19 kPa)、胸腔内压(6-8 kPa),显著优于商用产品 |
力学性能可编程调控:
通过调整打印结构的几何参数,可精准调控贴片的力学性能:
① 改变填充密度,可调控贴片的有效杨氏模量,实现从50 kPa到200 kPa的宽范围调整;
② 改变交替打印层之间的排列角度,可实现各向异性的力学性能,匹配不同组织的力学特性;
③ 受组织中波浪形胶原纤维启发,设计了波形打印结构,实现了与生物组织匹配的J型应力-应变曲线,可通过弯折角α精准调控应变硬化的转变点。
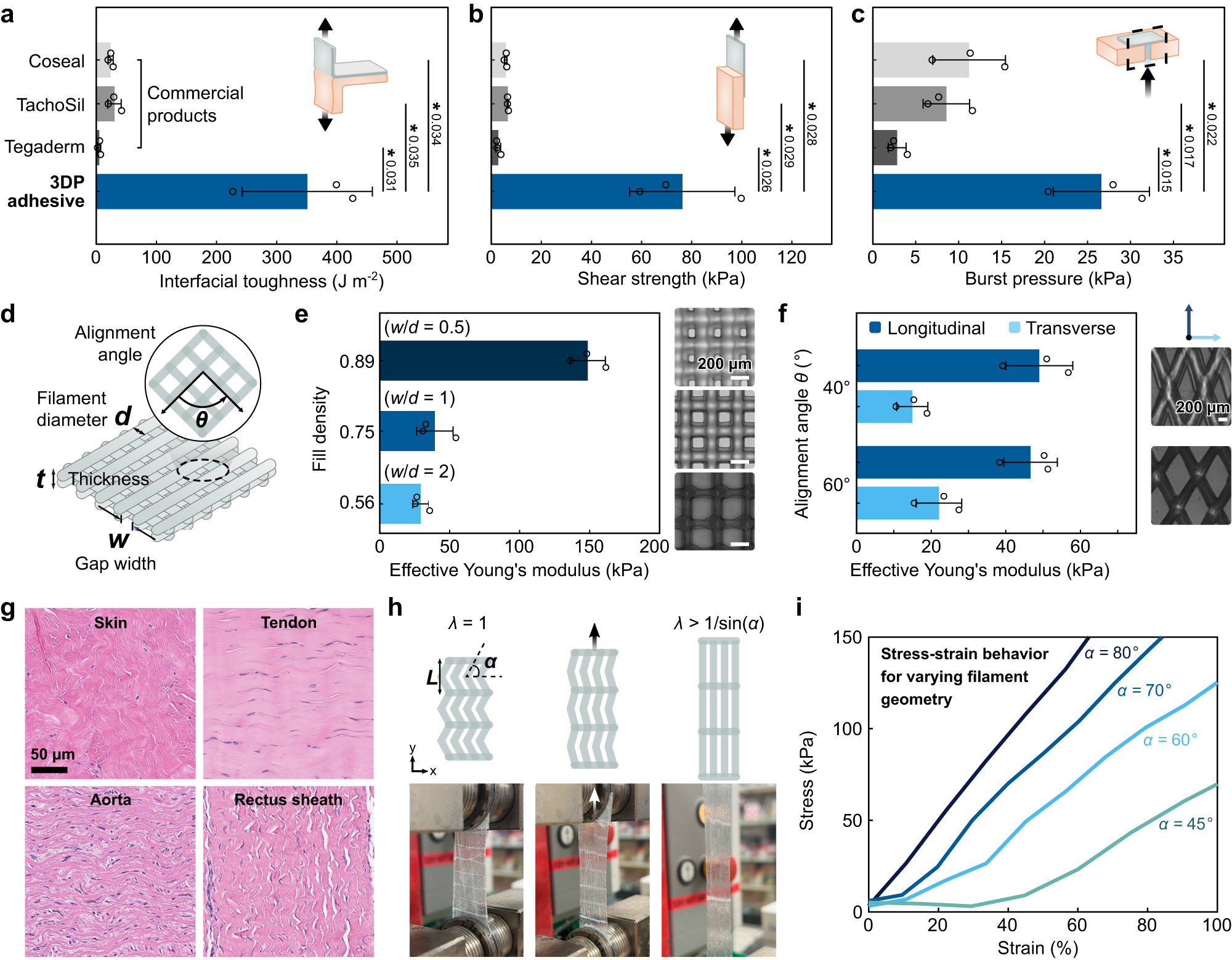
c:3D打印组织粘合剂与商用产品的爆破压力对比;
d:3D打印结构的可调几何参数;
e:不同填充密度的3D打印贴片的有效初始杨氏模量;
f:交替打印层之间不同排列角度的3D打印贴片的各向异性有效杨氏模量;
g:具有不同胶原纤维排列模式的各类猪组织的H&E染色组织学图像;
h-i:胶原纤维启发的波形结构贴片的单轴拉伸示意图与应力-应变曲线,验证了力学性能的可编程设计。
4. 生物相容性与体内修复效果验证
生物相容性与降解性:
① 体外细胞实验:小鼠成纤维细胞与打印贴片浸提培养基共培养,细胞活力与空白对照组无显著差异,与商用TachoSil、Coseal产品相当,无明显细胞毒性;
② 体内大鼠皮下植入实验:植入2周和4周后,贴片仅引发轻度炎症反应,4周时因水解降解植入物体积逐渐减小,炎症水平与降解性能与商用TachoSil相当,具备良好的体内生物相容性。
体内缺损修复效果:
构建了两种临床高难度的大鼠缺损模型,验证贴片的实际应用效果:
① 气管缺损模型:在大鼠气管构建2mm×1mm的椭圆形缺损,打印贴片仅需10秒轻柔按压即可实现气密密封,4周后缺损完全修复,无泄漏、无明显气管狭窄,贴片保持粘附且部分降解,仅伴轻度炎症;
② 结肠缺损模型:在大鼠结肠构建5mm切口缺损,贴片10秒内实现液密密封,4周后结肠缺损完全修复,无脓肿、无泄漏,贴片仍粘附于损伤部位并部分降解,解决了临床胃肠道缺损渗漏易引发感染、败血症的核心痛点。
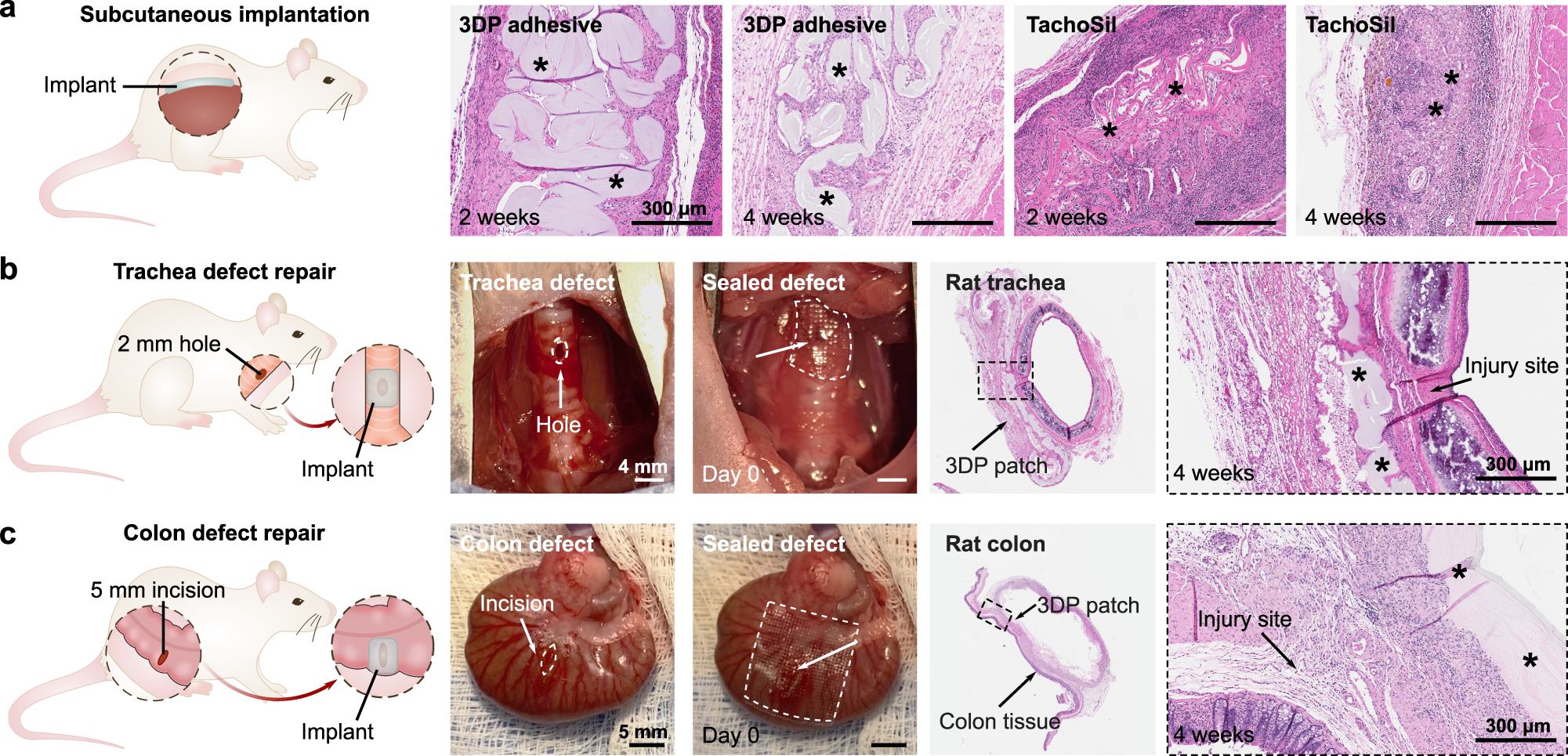
b:3D打印贴片修复大鼠气管缺损4周后的代表性照片与H&E染色组织学图像;
c:3D打印贴片修复大鼠结肠缺损4周后的代表性照片与H&E染色组织学图像;
组织学图像中*代表植入材料,所有动物模型均进行了3次独立实验,结果一致。
5. 抗出血粘附贴片设计与验证
针对血液环境下粘合剂易失效的临床难题,研究团队利用3D打印的设计自由度,开发了液体灌注抗血贴片:在3D打印多孔网格结构中整合胶原海绵,浸润疏水性油酸,构建了防血液浸润的粘附体系。
抗血粘附机制:疏水性液体形成物理屏障,阻止血液污染粘附界面;施加压力后,疏水性液体可通过网格孔隙排出,使粘合剂与组织直接接触,快速形成稳定粘附。
体内实验验证:该贴片可在10秒按压内,实现大鼠肝脏活动性出血缺损(5mm长、2mm深切口)、股动脉活动性出血缺损(约2mm切口)的快速止血与密封,解决了活动性出血创面难以粘附的行业痛点。

b:油灌注贴片粘附于浸没在血浴中的猪皮的照片;
c:抗血液、油去润湿与组织粘附过程的示意图;
d:油灌注3D打印贴片与涂油光滑贴片的爆破压力-施加压力对比,多孔打印贴片可在更低压力下实现更高的密封强度;
e-f:油灌注3D打印贴片修复大鼠肝脏、股动脉活动性出血缺损的体内应用照片,10秒按压即可实现止血密封。
6. 3D打印组织界面器件拓展应用
突破伤口闭合的单一应用,利用该3D打印平台,开发了多种一体化组织界面器件,拓展了应用边界:
① 生物电子贴片:3D打印一体化的粘附型生物电子贴片,集成LED电路,可稳定粘附于离体猪心脏,在心脏动态运动过程中保持电极与组织的紧密接触,LED持续点亮,为电生理信号传感与刺激的可穿戴/植入式器件提供了新方案;
② 图案化载药贴片:将模型药物(荧光素)直接混入打印墨水,实现了药物释放区域的精准空间图案化,可在粘附部位实现局部、定向的药物递送;
③ 可控释药储库贴片:打印了带可填充药物储库的粘附贴片,可通过调整界面孔隙尺寸调控药物释放速率,实现长效局部给药,降低全身给药的高剂量副作用。

c-d:负载模型药物(荧光素)的3D打印组织粘合剂贴片设计,以及在猪皮上的药物释放与扩散验证;
e-f:带可填充药物储库的组织粘合剂贴片设计,以及通过不同孔径界面调控药物释放的验证。






























