研究内容
1. 患者大脑3D重建与HiPGE蜂窝仿生设计
研究团队基于OASIS公开数据库中21名患者的MRI数据,通过3D Slicer软件重建了个体3D大脑模型,量化分析发现个体间脑尺寸、脑回复杂度存在极显著差异,直接证明了传统“一刀切”电极设计的局限性。
受天然蜂窝结构启发,团队设计了HiPGE蜂窝仿生可打印凝胶电极:采用六边形晶格单元,通过六重旋转对称实现各向同性弹性,多孔结构大幅提升了机械强度、柔性和曲面贴合性,同时可最大化皮层覆盖面积,不阻碍颅内液体交换,解决了传统ECoG电极阻碍脑脊液流动的问题。
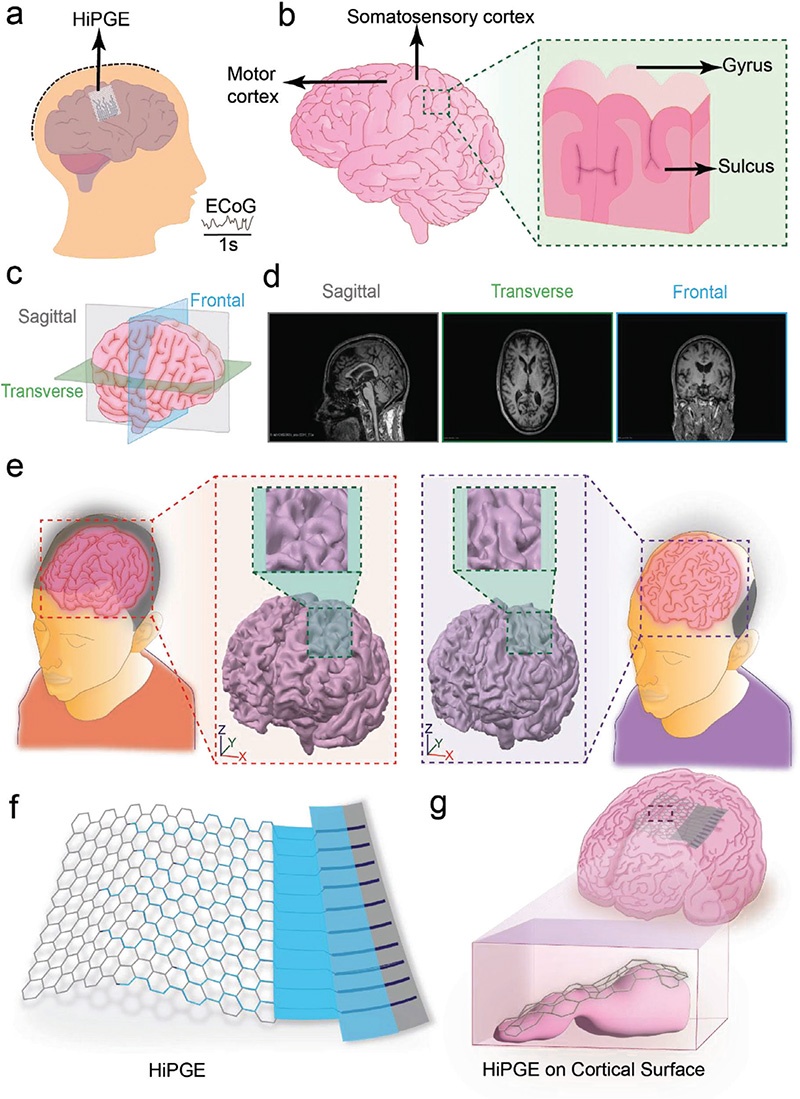
(a) 个性化HiPGE在体感皮层和运动皮层(指定ROI)进行ECoG记录的原理图;(b) ROI示意图,展示大脑皮层的脑回(gyrus)和脑沟(sulcus)解剖结构;(c,d) 三个解剖平面示意图(c),以及矢状面、横断面、额状面的MRI结构图像展示(d);(e) 不同个体皮层表面的差异展示,以及脑回结构的截面放大图(330号患者为左利手,349号患者为双利手);(f) HiPGE设计示意图;(g) 植入后贴合皮层表面的HiPGE侧视图。
2. FEA有限元分析引导的力学设计与性能评估
为实现与脑组织的力学性能精准匹配,团队通过有限元分析(FEA)对电极结构进行了系统优化,核心结果如下:
- 相同材料下,HiPGE的蜂窝结构比四边形多孔设计的弯曲刚度降低3倍,弯曲刚度与脑组织(0.1–10 kPa)高度匹配,远优于PDMS、SBS、金属等对照组;
- 贴合性仿真显示,HiPGE与脑组织的平均贴合距离仅2.66 mm,远优于PDMS对照组(4.16 mm)和SBS对照组(5.22 mm),同时对脑组织造成的应变变形最小;
- 电信号连通性仿真验证,HiPGE实现了近乎完美的电极连通率,远超非个性化、刚性对照组,彻底消除了接触不良导致的信号盲区。
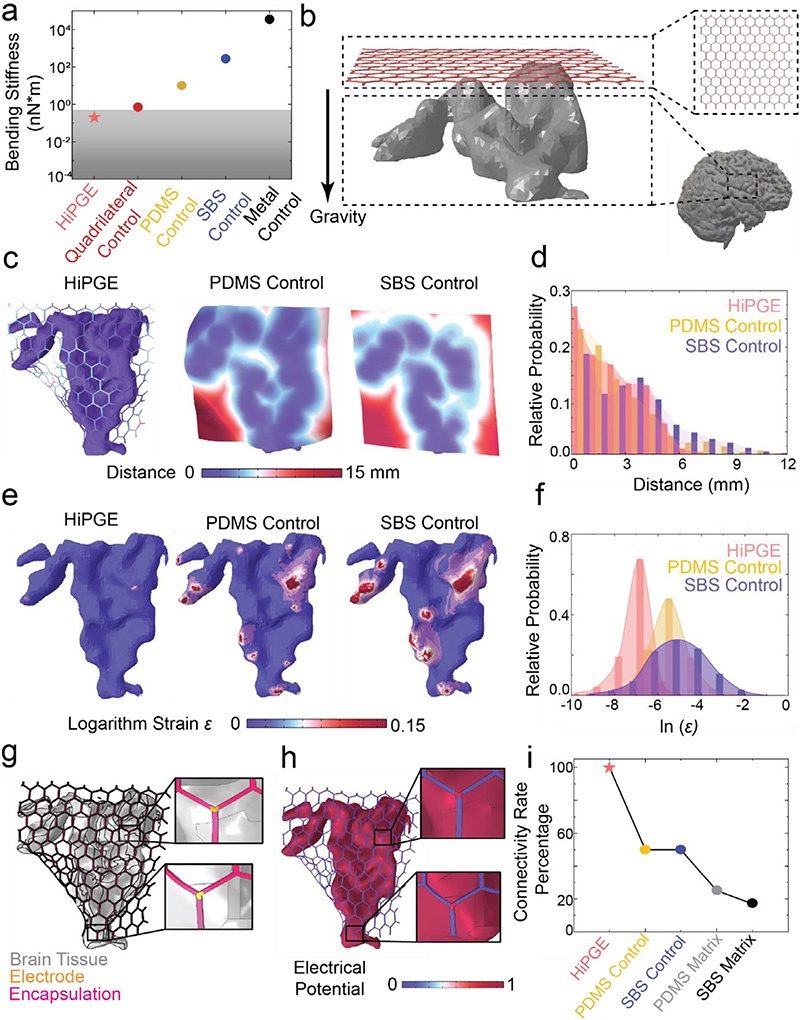
(a) HiPGE(粉色星标)、脑组织(灰色矩形)与其他对照器件的弯曲刚度对比;(b) 贴合性仿真设置示意图,HiPGE悬浮于MRI重建的3D大脑模型上方,通过重力沉降贴合脑表面;(c) 贴合性仿真后器件与脑组织贴合的最终构型,色阶图展示器件到脑表面的距离;(d) HiPGE与对照组的贴合距离分布概率直方图;(e) 贴合性仿真后变形的脑组织,色阶图展示脑组织上的对数应变分布;(f) HiPGE与对照组的对数应变分布概率直方图;(g) 脑表面HiPGE的仿真示意图;(h) 连通性仿真结果,HiPGE上的电极展现出良好的信号连通性;(i) 不同器件的信号连通率对比。
3. 基于直写式(DIW)3D打印的HiPGE制备与机械性能验证
HiPGE采用三明治结构设计:PDMS作为上下封装层,PEDOT:PSS/聚氨酯双连续导电聚合物水凝胶作为核心电极层。通过直写成型(DIW)3D打印技术实现一体化制备,打印分辨率可达100 µm。
团队随机选取5名患者的3D大脑模型,完成了定制化HiPGE的设计与打印,验证了电极位点可精准匹配个体脑回轮廓。机械性能测试显示,HiPGE的极限拉伸应变可达160%,具备优异的拉伸性和鲁棒性,可完美适配大脑的动态生理环境。
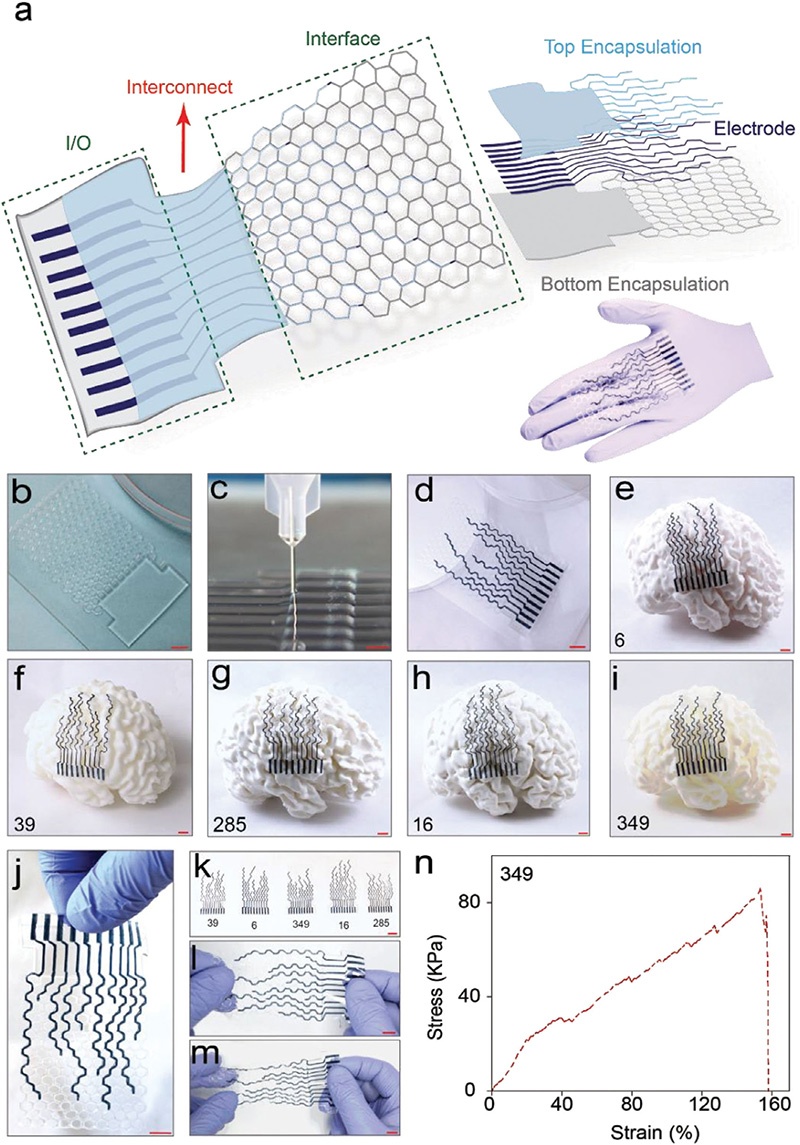
(a) HiPGE结构示意图(三层结构:底层、电极层、顶层;三个功能部分:界面区、互连区、I/O区)与3D打印实物照片;(b) 打印在玻璃基底上的单一个体器件底层照片;(c) 器件顶层打印过程图;(d) 打印在玻璃基底上的个性化HiPGE示意图;(e-i) 5款患者特异性HiPGE分别贴合对应患者大脑右半球模型的实物图(e-6号患者、f-39号患者、g-285号患者、h-16号患者、i-349号患者);(j) HiPGE易操作性展示;(k) 5款不同患者定制化HiPGE的设计与尺寸对比;(l-m) HiPGE未拉伸(l)与拉伸(m)状态的实物图;(n) 349号患者定制HiPGE的工程应力-应变曲线。
4. HiPGE电学性能系统表征
团队通过电化学测试全面评估了HiPGE的电学性能,核心结果如下:
| 测试项目 | 核心结果 | 性能优势 |
|---|---|---|
| 电化学阻抗谱(EIS) | 1-100000 Hz全频段内,阻抗均低于10 kΩ;100/1000 Hz下相位角接近0 | 阻抗比铂(Pt)、不锈钢(SS)对照电极低3-4个数量级,界面电荷传输能力优异 |
| 循环伏安(CV)测试 | 电荷存储容量(CSC)、电荷注入容量(CIC)均显著优于金属对照电极 | 源于导电水凝胶的离子-电子双传导机制、3D多孔结构超大界面面积与赝电容特性 |
| 长期稳定性测试 | 50℃ PBS加速老化28天(等效生理温度69天)、37℃人工脑脊液动态环境28天,性能无显著衰减 | 具备优异的长期使用稳定性,满足慢性植入需求 |
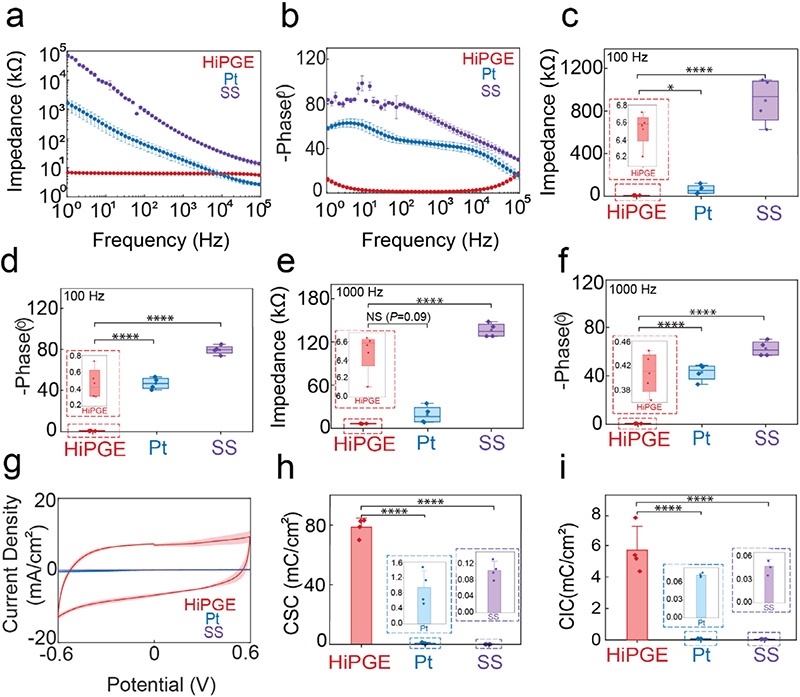
(a,b) HiPGE、铂(Pt)电极、不锈钢(SS)电极的电化学阻抗谱(EIS);(c-f) 100 Hz下的阻抗(c)与相位(d)、1000 Hz下的阻抗(e)与相位(f)对比;(g) HiPGE与对照电极的电流密度-电位曲线;(h,i) HiPGE与对照电极的电荷存储容量(CSC)(h)、电荷注入容量(CIC)(i)对比。
5. 大鼠在体功能验证
团队通过大鼠活体实验,完成了HiPGE的在体功能验证,实验采用同体对照设计:在大鼠视觉皮层双侧植入,左侧为定制化HiPGE,右侧为传统电极,在清醒大鼠中记录视觉诱发电位(VEP)。
核心实验结果:
- HiPGE记录的诱发电位信号质量显著优于传统电极,尤其是边缘通道的信号表现提升更为明显;
- 量化分析显示,HiPGE的信噪比(SNR)显著高于传统电极,边缘通道提升极显著(p<0.0001);
- 两种电极的峰潜伏期、振幅方差无显著差异,证明HiPGE在保证波形一致性的同时,大幅提升了神经信号采集的保真度。
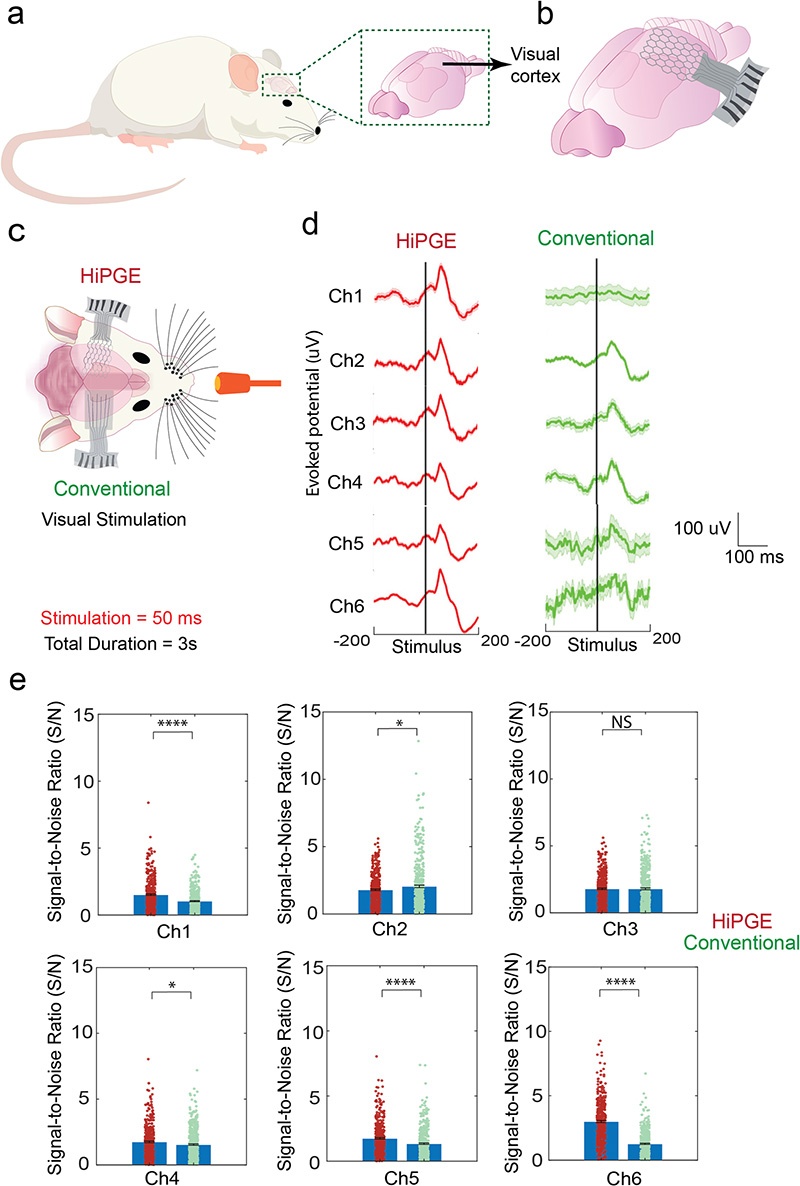
(a) 大鼠及其视觉皮层示意图;(b) 大鼠大脑视觉皮层植入HiPGE的示意图;(c) 同体实验设计示意图,左半球植入HiPGE,右半球植入传统电极,通过光刺激诱发皮层响应;(d) 清醒大鼠中HiPGE与传统电极记录的视觉诱发电位(VEPs),展示6个通道的试次平均波形;(e) 所有动物的信噪比(SNR)量化结果对比。
6. 组织形态完整性与生物相容性多模态评估
团队完成了HiPGE的MRI兼容性与长期生物相容性验证:
- MRI兼容性:7T小动物MRI扫描显示,植入HiPGE后,结构和功能MRI图像均无明显畸变或信号丢失,左右半球的信号强度无显著差异,可与MRI检查兼容使用。
- 长期生物相容性:植入4周后,组织学染色结果显示,HiPGE植入区无明显胶原纤维沉积(Masson染色)、无明显组织结构破坏(H&E染色)、小胶质细胞激活水平与非植入区无统计学差异(Iba-1染色),证明无明显免疫反应和瘢痕形成,具备优异的长期植入生物安全性。
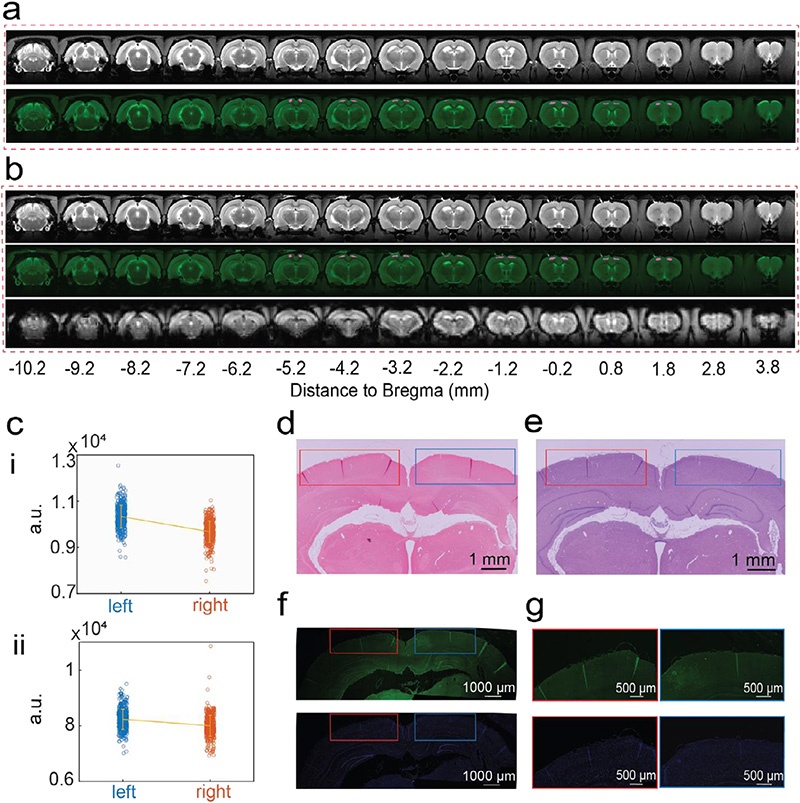
(a,b) 手术前(无HiPGE)(a)与手术后(植入HiPGE)(b)大鼠大脑的结构与功能MRI图像;(c) 手术前后大鼠左、右体感运动皮层的体素信号强度对比;(d-g) 植入4周后大鼠大脑的组织学染色结果:Masson三色染色(d)、H&E染色(e)、Iba-1/DAPI免疫荧光染色(f),以及植入区与非植入区的放大视图(g)。






























